Download hier de pdf van dit artikel
Desinfectiebijproducten in de waterzuivering
Het belang van schoon drinkwater werd duidelijk in 1854, toen John Snow ontdekte dat een vervuilde waterpomp de oorzaak was van een cholera-epidemie in Londen. Door chloor aan het water toe te voegen werd de infectie bestreden. Sinds die tijd heeft chloring van het drinkwater vele mensenlevens gered. In 1973 ontdekte Joop Rook echter dat er bij chloring van het drinkwater gechloreerde organische verbindingen kunnen ontstaan, die kankerverwekkend zijn [1]. Om die reden wordt chloring van het drinkwater in Nederland alleen nog toegepast in geval van calamiteiten. UV-straling bleek een goed alternatief te zijn om pathogenen te inactiveren. De laatste jaren worden er steeds meer (antropogene) organische stoffen aangetroffen in bronnen voor drinkwater, deels doordat er steeds meer stoffen worden toegepast, deels ook door verbeterde analysetechnieken. Hierdoor is het mogelijk heel lage concentraties en meer polaire verbindingen te detecteren. UV-straling, in combinatie met waterstofperoxide, blijkt een effectieve methode om dergelijke organische microverontreinigingen af te breken [2].

Geavanceerde oxidatie wordt op verschillende locaties ingezet bij de productie van drinkwater voor de verwijdering van organische microverontreinigingen. Bij behandeling van water met geavanceerde oxidatie kunnen soms ongewenste bijproducten ontstaan, die mutagene activiteit vertonen [3,4]. Of een monster mogelijk mutagene verbindingen bevat, kan worden bepaald met behulp van een zogenaamde Ames-fluctuatietest (zie kader). Als een stof in de Amestest een respons geeft, wil dat niet automatisch zeggen dat die stof ook voor mensen schadelijk is. Daarom werd de respons van deze Amestest in eerder onderzoek [5] vertaald in zogenaamde 4-nitroquinoline-oxide (4-NQO)-equivalenten. 4-NQO is een bekende genotoxische verbinding, die vaak als positieve controle in de Amestest wordt toegepast. De grens waaronder het risico van de aanwezige mutagene verbindingen in drinkwater verwaarloosbaar wordt geacht (de zogenoemde Threshold of Toxicological Concern of TCC) is voor genotoxische verbindingen gesteld op 10 ng/L. Het bleek dat UV-behandeling van kunstmatig samengesteld water met middendruk (MD) lampen leidde tot de vorming van 120 ng/L 4-NQO-equivalenten. Dit illustreert dat de gevormde verbindingen van gezondheidskundig belang kunnen zijn [5]. Het daadwerkelijke risico van een gevormd bijproduct kan alleen met behulp van stofspecifieke toxicologische studies worden vastgesteld als de identiteit van de verbinding bekend is. Er is nog niet zoveel bekend over de identiteit van de bijproducten die gevormd worden onder invloed van UV-straling, maar inmiddels wel over de factoren die bijdragen aan hun vorming. Ook is aangetoond dat tijdens vervolgstappen in de drinkwaterbereiding (zoals actieve kool of duinpassage) de eventuele mutagene activiteit weer verwijderd wordt [3].

Het is belangrijk om de identiteit van de gevormde bijproducten te kennen en te weten onder welke omstandigheden ze gevormd worden. Met die kennis kunnen de verbindingen tijdens de drinkwaterbehandeling worden opgespoord en kan mogelijk hun vorming voorkomen worden. Dat is altijd beter dan gevormde producten te moeten verwijderen. Bovendien is de identiteit van een bijproduct nodig om het risico voor de volksgezondheid te kunnen vaststellen. Om deze kennishiaten te vullen is er binnen het bedrijfstakonderzoek (BTO) van de Nederlandse drinkwaterbedrijven onderzoek uitgevoerd naar factoren die invloed hebben op de vorming van bijproducten [6] en is er een analytisch-chemische tool ontwikkeld. Deze laatste is gebaseerd op het labelen met stabiele isotopen [7]. Dit artikel vat de resultaten van beide studies samen.
Factoren die invloed hebben op vorming bijproducten
Ten eerste is in het BTO vastgesteld welke factoren van invloed zijn op de vorming van bijproducten tijdens UV-bestraling [6]. Onderzoek in allerlei verschillende desinfectie-installaties voor drinkwater toonde aan dat de hier toegepaste lage doses geen mutagene bijproducten opleveren. Voor het onderzoek naar het effect van hogere doses werd uitgegaan van voorbehandeld drinkwater, waarvan de concentraties natuurlijk organische materiaal en zouten werden aangepast. De volgende factoren bleken invloed uit te oefenen op de mutagene activiteit die met de Ames-fluctuatietest werd bepaald:
Het type UV-lamp
Over het algemeen worden er twee typen UV-lampen toegepast voor waterbehandeling. Lage druk-(LD)-lampen zenden straling uit met een golflengte van 254 nm. MD-lampen zenden een breed scala aan golflengtes uit tussen 200 en 300 nm. Deze lampen zijn daardoor veel effectiever om fotolyse te bewerkstelligen, maar juist dit proces lijkt de vorming van mutagene bijproducten te veroorzaken. De vorming van mutagene bijproducten kan worden beperkt wanneer het gebruik van golflengten tussen circa 200 en 240 nm wordt vermeden. Dit heeft geen gevolgen voor de zuiveringsefficiëntie van het totale proces.
De toegepaste UV-dosis
Mutagene bijproducten worden niet gedetecteerd bij de lage UV-doses die bij desinfectie van drinkwater worden toegepast. Bij hogere doses, zoals tijdens geavanceerde oxidatieprocessen, neemt de kans op de vorming van dergelijke bijproducten met toenemende dosis toe.
De samenstelling van het water
Het type en de concentratie aan natuurlijk organisch materiaal (NOM) en de concentratie nitraat in het water zijn van invloed op de vorming van mutagene bijproducten. Bij hogere concentraties van NOM en nitraat is een hogere respons in de Ames-fluctuatiestest gemeten. Dit wordt verklaard doordat de mutagene bijproducten worden gevormd door fotolyse van nitraat en de reactie van de resulterende verbindingen met NOM of reactieproducten daarvan. Doordat alleen MD-lampen fotolyse van nitraat kunnen bewerkstelligen, bij een golflengte <240 nm, treedt het effect op bij deze lampen.
De H2O2-concentratie
Waterstofperoxide (H2O2) bevordert het oxidatieproces en lijkt de vorming van mutagene bijproducten tegen te gaan. Mogelijk komt dit doordat het H2O2 een deel van de UV-straling afvangt. Daarnaast breken de gevormde hydroxylradicalen de onder invloed van UV gevormde bijproducten mogelijk weer af. Dit wijst erop dat inderdaad fotolyse verantwoordelijk is voor de vorming van mutagene bijproducten.
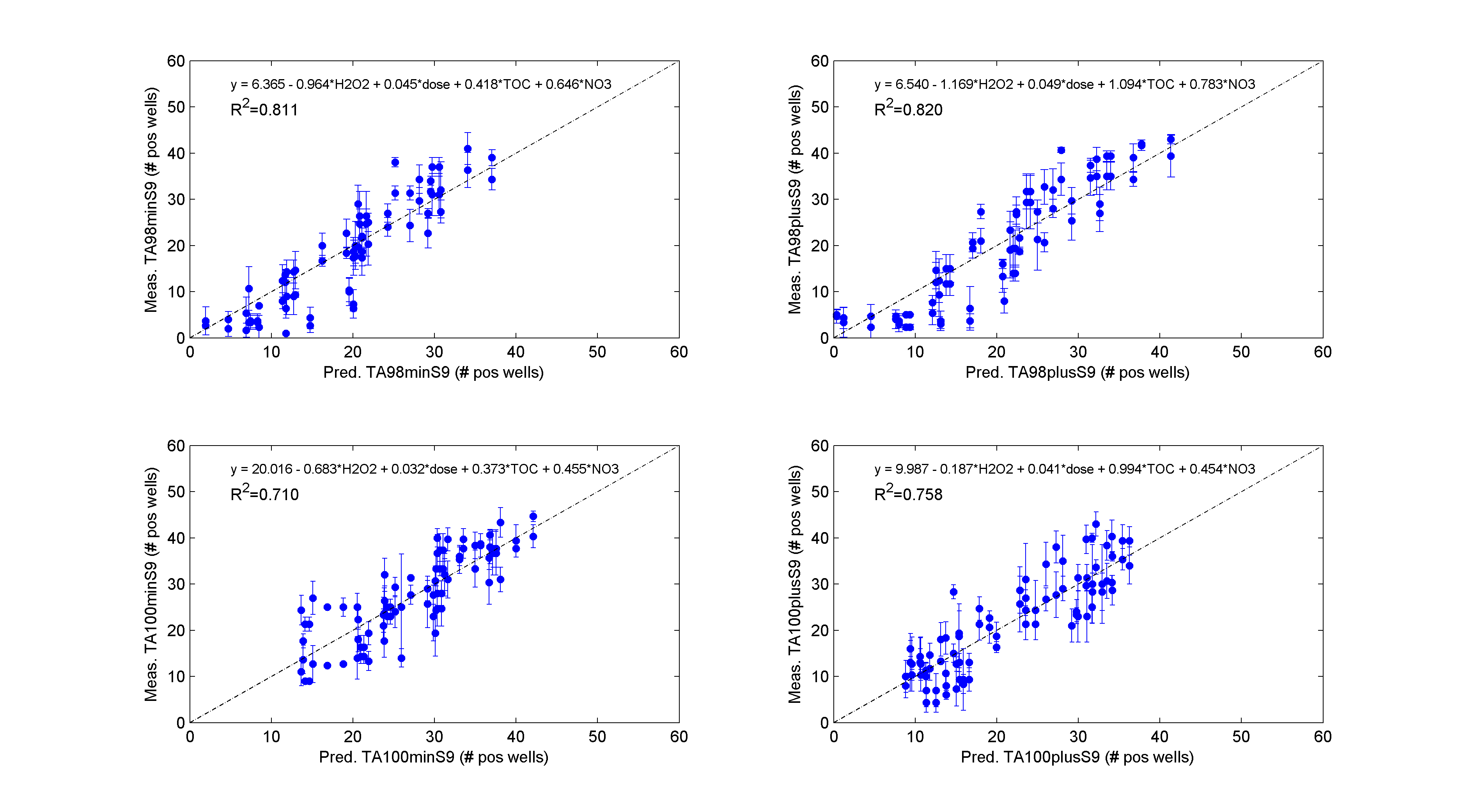 Afbeelding 1: wiskundige beschrijving van de relatie tussen de Ames-respons en diverse factoren die hierop van invloed zijn bij toepassing van een MD-UV-lamp (H2O2-concentratie, UV-dosis, TOC-gehalte (totale gehalte aan organisch materiaal) en nitraatconcentratie). Er zijn twee bacteriestammen gebruikt (TA98 en TA100) en hieraan is wel of niet S9 toegevoegd. S9 is een leverextract, dat het effect van metabolisme van de stofjes op de mutageniteit laat zien
Afbeelding 1: wiskundige beschrijving van de relatie tussen de Ames-respons en diverse factoren die hierop van invloed zijn bij toepassing van een MD-UV-lamp (H2O2-concentratie, UV-dosis, TOC-gehalte (totale gehalte aan organisch materiaal) en nitraatconcentratie). Er zijn twee bacteriestammen gebruikt (TA98 en TA100) en hieraan is wel of niet S9 toegevoegd. S9 is een leverextract, dat het effect van metabolisme van de stofjes op de mutageniteit laat zien
Analytisch-chemische tool voor opsporen bijproducten van MP-UV
Uit het bovengenoemde onderzoek en uit kennis uit de literatuur valt af te leiden dat bijproducten bestaan uit organische verbindingen die worden gevormd tijdens fotolyse van nitraat en de reactie met het aanwezige NOM of (fotolyse)producten daarvan. Gebruik makend van deze kennis is er binnen het BTO een innovatieve analytisch-chemische methode ontwikkeld om de bijproducten te traceren [7]. De methode maakt gebruik van stabiele isotopen in combinatie met een hoge-resolutie-massaspectrometrie.
Kunstmatig water met gelabeld nitraat en hoge-resolutie-massaspectrometrie
Voor het onderzoek is gebruik gemaakt van nitraat, gelabeld met een stabiele N15-isotoop. In het laboratorium werd kunstmatig water gemaakt door NOM en nitraat op te lossen in ultrapuur water. Het water werd met behulp van een MD-lamp bestraald in een zogeheten collimated beam-opstelling, waarmee in het laboratorium onder goed gedefinieerde omstandigheden UV-experimenten kunnen worden uitgevoerd. Wanneer gelabeld nitraat reageert met een organische verbinding waarbij het stikstofatoom in het molecuul wordt ingebouwd, is het massaverschil met een niet-gelabelde verbinding 0,99704 Dalton. Met behulp van vloeistofchromatografie gekoppeld aan hoge-resolutie-massaspectrometrie (LC-HR-MS) is een dergelijk verschil goed te detecteren (zie afbeelding 2).
Om lage concentraties van gevormde stikstofhoudende bijproducten te analyseren, zijn concentratie en monstervoorbehandeling middels vaste fase-extractie (SPE) toegepast. Vervolgens is met behulp van LC-HR-MS een brede screening [8] uitgevoerd op de watermonsters. Met behulp van HR-MS kan de brutoformule van een stof worden bepaald op basis van de accurate massa van een component en kunnen onbekende componenten worden geïdentificeerd.
 Afbeelding 2: opzet stikstoflabeling-experiment
Afbeelding 2: opzet stikstoflabeling-experiment
84 stikstofhoudende bijproducten gevormd in kunstmatig water
Uit het onderzoek bleek dat er 84 verbindingen in het water werden gevormd door reactie met nitraat tijdens de bestraling. Drie hiervan, 4-nitrofenol, 4-nitrocatechol en 2-methoxy-4,6-dinitrofenol, konden worden geïdentificeerd. Verder bestaat het sterke vermoeden dat ook 2-hydroxy-5-nitrobenzoëzuur, 5-nitrovaniline, 4-nitroftaalzuur, nitrobenzeensulfonzuur en 2,4-dinitrofenol werden gevormd. Van de drie geïdentificeerde verbindingen zijn weinig of geen toxicologische gegevens bekend. 4-nitrofenol lijkt in de Amestest niet mutageen te zijn. Op basis van zijn structuur is van 2-methoxy-4,6-dinitrofenol wel te verwachten dat die verbinding een positieve Ames-respons zou veroorzaken.
Screening van bijproducten in praktijkmonsters
Vervolgens werden watermonsters uit een full-scale drinkwaterzuiveringsinstallatie op basis van MP-UV/H2O2-behandeling onderzocht op de 84 verbindingen die in het kunstmatige water waren aangetoond. Het bleek dat 22 van deze stoffen inderdaad ook in het bestraalde water konden worden aangetoond. Ook de drie geïdentificeerde verbindingen behoorden hiertoe. De totale concentratie bleek echter een factor 9 lager te zijn in de full-scale installatie dan in het kunstmatige water was aangetroffen. Dit kan komen door de samenstelling van het NOM in het praktijkwater, dat anders is dan het Pony Lake-NOM uit het kunstmatige water. Bovendien is op het laboratorium geen waterstofperoxide toegevoegd, terwijl dat in de full-scale praktijkinstallatie wel het geval was. Zoals hierboven al vermeld, leidt de aanwezigheid van H2O2 tot een lagere respons in de Amestest [5].
Om uit te zoeken of deze 22 bijproducten verantwoordelijk zijn voor de mutageniteit die wordt waargenomen na geavanceerde oxidatie, werd ook de Ames-fluctuatietest uitgevoerd op deze monsters. Bovendien werden de chemische analyse en de Amestest ook uitgevoerd aan het einde van het drinkwaterzuiveringsproces (na duininfiltratie). De vergelijkbare trends van de chemische screening en de mutagene respons in deze praktijkmonsters, tonen aan dat (een deel van) deze 22 bijproducten kunnen bijdragen aan de waargenomen mutageniteit. Vervolgonderzoek is nodig om de identiteit van alle gedetecteerde verbindingen te achterhalen en de relatie te leggen met de mutagene respons, bijvoorbeeld met behulp van ‘effect directed’-analyse. Daarnaast kunnen de lotgevallen van de gevormde bijproducten tijdens vervolgstappen in de drinkwaterzuivering nu gevolgd worden. Dit type studies kan helpen een verantwoorde toepassing van UV-processen bij diverse watertypen en in diverse zuiveringsschema’s te bewerkstelligen.
Conclusie
De twee studies hebben meer inzicht gegeven in de factoren die invloed hebben op de vorming van mutagene bijproducten in UV-processen, namelijk het type UV-lamp, de toegepaste UV-dosis, de concentratie nitraat, de concentratie NOM, en de toevoeging van H2O2. Het blijkt dat toepassing van hoge doses MD-UV-straling kan leiden tot de vorming van stikstofhoudende bijproducten, die ontstaan door fotolyse van nitraat en reactie van de resulterende verbindingen met NOM of reactieproducten daarvan. Door gebruik te maken van gelabeld stikstof in het nitraat, is het mogelijk gevormde bijproducten te traceren. Deze innovatieve tool voor het opsporen en identificeren van bijproducten die gevormd worden tijdens geavanceerde oxidatieprocessen, is een belangrijke stap voorwaarts om inzicht te krijgen in (i) de mechanismen van de vorming, (ii) het gedrag van de gevormde bijproducten tijdens drinkwaterzuivering en (iii) de humane risico’s van deze bijproducten. Deze nieuwe kennis maakt het mogelijk te achterhalen welke potentieel mutagene bijproducten bij geavanceerde oxidatie kunnen worden gevormd, met als uiteindelijk doel het ontstaan van deze verbindingen zoveel mogelijk te voorkomen. Deze studies helpen drinkwaterbedrijven die geavanceerde oxidatie willen toepassen, om de veiligheid van het drinkwater in alle stappen van hun productieproces te bewaken.
Referenties
- Rook, J. J., Formation of haloforms during chlorination of natural waters. Water Treatment Examination 1973, 23, (234).
- Wols, B.A., Hofman-Caris, R.C.H.M., Harmsen, D.J.H., Beerendonk,. E.F., Degradation of 40 selected pharmaceuticals by UV/H2O2. Wat. Res. 2013, 47 (15), 5876-5888
- Heringa, M. B., Harmsen, D. J. H., Beerendonk, E. F., Reus, A. A., Krul, C. A. M., Metz, D. H., Ijpelaar, G. F., Formation and removal of genotoxic activity during UV/H2O2-GAC treatment of drinking water. Water Research 2011, 45, (1), 366-374.
- Martijn, A. J., Boersma, M. G., Vervoort, J. M., Rietjens, I. M. C. M., Kruithof, J. C., Formation of genotoxic compounds by medium pressure ultraviolet treatment of nitrate-rich water. Desalination and Water Treatment 2014, 52, 6275-6281.
- Martijn, A. J., Kruithof, J. C., Hughes, R. A. M., Mastan, R. A., Van Rompay, A. R., Malley jr., J. P., Induced genotoxicity in medium pressure UV treated nitrate rich water. Journal - American Water Works Association 2015, 107.
- Hofman-Caris, R. C. H. M., Harmsen, D. J. H., Puijker, L., Baken, K. A., Wols, B. A., Beerendonk, E. F., Keltjens, L. L. M., Influence of process conditions and water quality on the formation of mutagenic byproducts in UV/H2O2 processes. Water Research 2015, 74, 191-202.
- Kolkman, A., Martijn, B. J., Vughs, D., Baken, K. A., van Wezel, A. P., Tracing nitrogenous disinfection byproducts after medium pressure UV water treatment by stable isotope labeling and high resolution mass spectrometry. Environmental science & technology 2015, 49, (7), 4458-4465.
- Leerdam, T. van, Bajema, B., de Graaf, B., van der Kooi, J., Puijker L., Brede chemische screening voor het monitoren van de waterkwaliteit. H2O, 2015.


















